Por: Nina Padme Eufracio Rojas / Departamento de Químico en Fármacos. Centro de Enseñanza Técnica Industrial Plantel Colomos. C.. Nueva Escocia 1885, 44630 Guadalajara, Jal. Correo : neufraciorojas@gmail.com / Instagram:@ninapadme
Una gota cae sobre una superficie al rojo vivo. En lugar de evaporarse al instante, como cabría esperar, empieza a temblar, deslizarse, a moverse erráticamente como si danzara. Lejos de desaparecer, se vuelve inquieta, rápida y escurridiza. Lo que ocurre ahí no es simple evaporación, sino un fenómeno físico extraordinario conocido como efecto Leidenfrost, que convierte el calor extremo en un escenario para el movimiento elegante de las moléculas.

Este efecto se manifiesta cuando un líquido entra en contacto con una superficie cuya temperatura supera significativamente su punto de ebullición, creando una capa de vapor entre ambos que impide el contacto directo. A primera vista, parecería que el calor debería intensificar la evaporación, pero ocurre lo contrario: la gota se mantiene entera más tiempo de lo esperado. ¿Por qué? Porque la base de la gota, al tocar la superficie muy caliente, se vaporiza tan rápidamente que forma una burbuja de gas que levanta el resto del líquido, evitando que el calor penetre de inmediato. La gota, entonces, levita sobre su propio vapor.
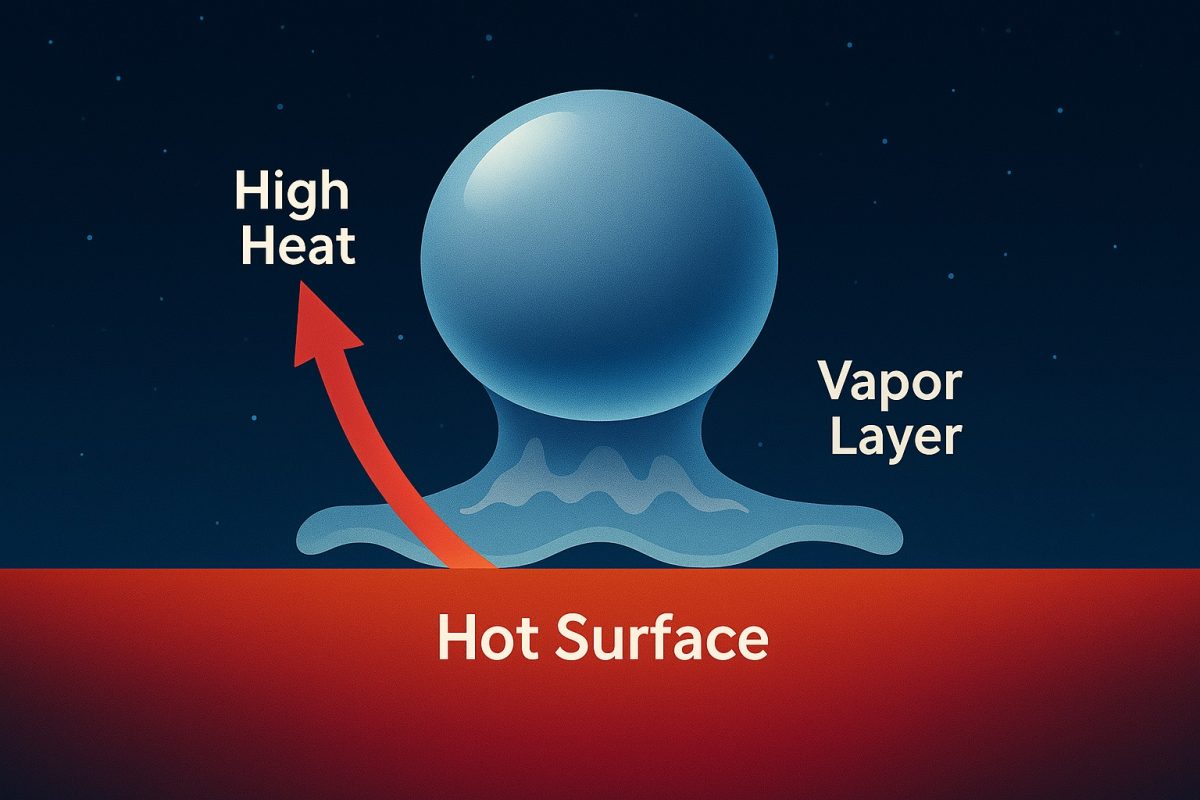
Desde un punto de vista molecular, lo que ocurre es fascinante. La energía térmica de la superficie provoca una vaporización ultra rápida en la base del líquido. Este vapor, al expandirse, genera una presión ascendente que separa físicamente la gota de la superficie caliente. Así, el resto del líquido se mantiene aislado, y el calor ya no se transfiere por conducción sólida, sino a través del vapor —un mecanismo mucho menos eficiente—, ralentizando notablemente la evaporación. Pero eso no es todo. La forma en que las moléculas se comportan dentro de este sistema es única. El vapor actúa como un escudo térmico, y además, como un lubricante dinámico. En este colchón de gas, la gota no solo levita: adquiere gran movilidad, se desliza a velocidades altas por pequeños desniveles de la superficie, respondiendo a variaciones de temperatura, inclinación o textura. Su comportamiento se vuelve tan sensible que puede incluso usarse para mover gotas a voluntad, sin contacto físico, solo manipulando la geometría térmica del entorno.
Este fenómeno, descrito por primera vez en 1756 por Johann Gottlob Leidenfrost, hoy se estudia con técnicas modernas como cámaras de ultra alta velocidad, espectroscopía térmica y simulaciones moleculares. Sabemos que la temperatura crítica varía según el líquido: en el caso del agua, ronda los 200 a 250 °C, dependiendo de la presión atmosférica y la pureza del líquido. Para líquidos más volátiles, como etanol o acetona, el efecto ocurre a temperaturas más bajas.
Lo más intrigante del efecto Leidenfrost es su versatilidad: no solo ocurre con agua, sino también con alcoholes, refrigerantes industriales, nitrógeno líquido, e incluso en experimentos con metales fundidos. Esto lo convierte en un modelo físico para estudiar interacción térmica extrema en múltiples disciplinas: desde ingeniería térmica hasta biotecnología, desde astrobiología hasta microfluidos.
Además, las implicaciones prácticas son sorprendentes. En materiales diseñados para operar en ambientes de alta temperatura, como turbinas, hornos industriales o reactores, comprender el efecto Leidenfrost permite desarrollar revestimientos que reducen la degradación térmica. En laboratorios de química y biología, se ha explorado su uso en plataformas de manipulación de gotas sin contacto, evitando contaminación cruzada o pérdidas por evaporación. Incluso en astrofísica experimental, se estudia su papel potencial en entornos planetarios extremos donde los líquidos pueden existir momentáneamente sobre superficies supercalientes.
Lo que hace tan especial a este fenómeno es que la levitación no depende de una fuerza externa, sino del equilibrio entre vaporización y presión interna, de una coreografía espontánea entre energía, fase gaseosa y estructura líquida. La gota no necesita alas: se sustenta en su propio aliento.
Y si una gota puede danzar en esas condiciones, entonces las moléculas no solo resisten al calor, sino que también aprenden a moverse en él. Aprenden a sobrevivir flotando sobre lo que normalmente las destruiría.
Como todo en la ciencia, esto no es solo un fenómeno… es una metáfora elegante de la adaptación molecular bajo presión.
Referencias
- Celestini, F., & Kirstetter, G. (2012). Effect of the Leidenfrost phenomenon on heat transfer. Journal of Heat Transfer, 134(4), 041501. Recuperado de: https://asmedigitalcollection.asme.org/heattransfer/article/134/4/041501/468623
- Bormashenko, E. (2017). Why Leidenfrost effect is so fascinating? Colloids and Surfaces A, 519, 116–122. Recuperado de: https://www.sciencedirect.com/science/article/abs/pii/S0927775717300847
- Biance, A.-L., Clanet, C., & Quéré, D. (2003). Leidenfrost drops. Physics of Fluids, 15(6), 1632–1637. Recuperado de: https://pubs.aip.org/aip/pof/article/15/6/1632/251615/Leidenfrost- drops
- Maquet, L., & Fort, E. (2016). Leidenfrost dynamics on textured surfaces. Scientific Reports, 6, 32130. Recuperado de: https://www.nature.com/articles/srep32130
- Linke, H., Aleman, B. J., Melling, L. D., et al. (2006). Self-propelled Leidenfrost droplets. Physical Review Letters, 96(15), 154502. Recuperado de: https://journals.aps.org/prl/abstract/10.1103/PhysRevLett.96.154502
- Lagubeau, G., Le Merrer, M., Clanet, C., & Quéré, D. (2011). Leidenfrost on a ratchet. Nature Physics, 7(5), 395–398. Recuperado de: https://www.nature.com/articles/nphys1925
- Soto, D., & Bird, J. C. (2015). Leidenfrost droplets on curved surfaces. Journal of Fluid Mechanics, 746, 365–386. Recuperado de: https://www.cambridge.org/core/journals/journal-of-fluid- mechanics/article/leidenfrost-droplets-on-curved- surfaces/44C5E4F5B1405DA48F9F6BB2ED34C2C2
- Shirota, M., van Limbeek, M. A. J., Sun, C., Prosperetti, A., & Lohse, D. (2016). Dynamic Leidenfrost effect: relevant time and length scales. Physical Review Letters, 116(6), 064501. Recuperado de: https://journals.aps.org/prl/abstract/10.1103/PhysRevLett.116.064501
- Vakarelski, I. U., Marston, J. O., Chan, D. Y. C., & Thoroddsen, S. T. (2012). Drag reduction by Leidenfrost vapor layers. Nature, 489(7415), 274–277. Recuperado de: https://www.nature.com/articles/nature11418
- Xu, X., Ma, X., Zhao, Y., et al. (2022). Superwetting Leidenfrost effect for heat management. ACS Nano, 16(1), 556–566. Recuperado de: https://pubs.acs.org/doi/10.1021/acsnano.1c06039
Otras entradas de esta sección
- Las cianobacterias, el secreto de la vida en la Tierra
- Moléculas en el espacio: ¿Qué pistas nos dan?
- Criopreservación : ¿Cómo sobreviven las células a temperaturas extremas?
- Fotosíntesis Basada en Metano para la Generación de Energía en Ambientes Extraterrestres
- Venenos Letales del Océano
- El Último Viaje del Silicio en el Universo
- Cromatóforos y el Camuflaje de los Cefalópodos
- Las Moléculas Giratorias del Espín Molecular
- Las Proteínas Adhesivas de los Mejillones
- Arsénico en las Profundidades
- Efecto Marangoni en Burbujas Dinámicas
- Secreto Químico del Chile Mexicano
- Moléculas antifúngicas de los Maíces Criollos
- El efecto Zeeman en nebulosas magnéticas
- Cavidades supramoleculares en asteroides
- Interacciones no covalentes en la formación de compuestos pre-bióticos
- El efecto Leidenfrost en interfaces térmicamente extremas
